В химическом процессе массы веществ перед химическим процессом равны массе веществ после процесса. Поэтому химические процессы, также называемые химическими реакциями, можно представлять в виде уравнений. Их называют химическими уравнениями или уравнениями химической реакции. В химических уравнениях знак равенства заменяется стрелкой. В левой части уравнения указываются исходные вещества, в правой — возникающие после реакции вещества (конечные вещества). Количество атомов слева от стрелки должно совпадать с количеством атомов справа от стрелки. Если проверка показывает, что необходимо
|
выравнивание, оно представляется соответствующим числом перед условным знаком (рис. 14.21). 14.1.4.6. Синтез, анализ Под синтезом понимают производство химического соединения. Производство синтетических материалов, например пластмасс, является одной из основных задач химической промышленности. Разложение химического соединения на его элементы называют анализом. Синтез и анализ — это химические процессы. Они могут представляться химическими уравнениями (рис. 14.22). 14.1.5. Смеси Некоторые вещества можно смеши вать сколько угодно друг с другом, но при этом эти вещества не образуют химические соединения. Возникающая смесь не является новым веществом. Потом ее можно снова разделять физическими процессами в исходные вещества, например дистилляцией, испарением, фильтрованием, магнитным разделением или осаждением. Смесями являются, например, растворы, дисперсии и сплавы. 14.1.5.1. Растворы Многочисленные твердые, жидкие и газообразные материалы можно распределять в жидкостях настолько тонко, что останутся только лишь отдельные молекулы или ионы. Вещества в таком случае находятся в растворе. Жидкость называют растворителем (рис. 14.23). Определенное количество растворителей может растворить при определенной температуре только ограниченное количество материала. Если это состояние достигнуто, раствор насыщен. Близкий к насыщению раствор называют сконцентрированным, раствор с концентрацией намного ниже, чем концентрации насыщения, — разбавленным. Процесс растворения можно ускорять измельчением растворяемого материала, а также перемешиванием или нагреванием. Растворяемые твердые материалы могут выделяться из растворов испарением или испарением растворителя, например при высыхании лаков. Для разделения двух растворенных друг в друге жидкостей используют дистилляцию раствора. |
|
Исходные |
Химический ——- ——► |
Конечные |
|
вещества |
процесс |
вещества |
|
Примеры: 2Н2 + водород |
|
кислород 2HCI — |
|
2Н20 вода |
|
ZnCI2 хлорид цинка |
|
+ Н2 водород |
|
Zn + цинк 4Fe + железо |
|
соляная кислота |
|
зо2 — кислород |
|
2Fe203 оксид железа |
|
Пример синтеза: |
||
|
> + со О |
——————- ► |
2А12Оз |
|
алюминии кислород |
ОКСИД алюминия |
|
|
Пример анализа: |
||
|
2НдО ——————— ► |
2Нд + |
о2 |
|
ОКСИД ртути |
ртуть |
кислород |
|
Рис. 14.21. Химические уравнения |
|
Рис. 14.22. Синтез и анализ |
|
о Растворитель О Молекулы растворенного вещества |
||
|
в? т О ( ) О О О о Vo vS •Уі* о°°° о:’ ®’С °°о п° ° о О Л ©Л® ® о® 9«^ о*. Л» О® © ® |
||
|
Рис. 14.23. Раствор |
|
|
|
|
|
Рис. 14.26. Дистилляция |
|
14.1.5.3. Сплавы В жидком состоянии большинство металлов можно растворить друг в друге. Застывший раствор следует называть сплавом. При этом свойства сплава часто значительно отличаются от свойств содержащихся в нем отдельных веществ, например по их прочности и температуре плавления. Производством расплава можно изготавливать производственные материалы с определенными свойствами, например после легирования хромом и никелем сталь становиться коррозионностойкой. |
Раствор доводится до кипения. Кипящая при более низкой температуре жидкость легче испаряется и снова сжижается охлаждением. Жидкость, кипящая при более высокой температуре, остается в сосуде. Разделение нескольких растворимых жидкостей производится многократной дистилляцией, при этом жидкости испаряются при достижении соответствующей точки кипения и улавливаются отдельно. При этом говорят о фракционированной дистилляции, которая применяется, например, для разложения нефти на бензин, жидкое топливо, смазочное масло и битум.




 11 января, 2015
11 января, 2015 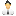 Furniturer
Furniturer 
 Опубликовано в рубрике
Опубликовано в рубрике